一、實驗部分
(一)儀器與原料
自制不銹鋼立式種分槽(2L)(中南大學機械廠),JS94H微電泳儀(上海中晨數字技術設備有限公司),DT-102型全自動界面張力儀(淄博華坤電子儀器有限公司)。
鋁酸鈉溶液采用工業氫氧化鈉和工業氫氧化鋁配制而成,分子比為1.45~1.50,氧化鋁濃度為165~185g/L。所加晶種為經80~100℃干燥的工業氫氧化鋁。
實驗所加入的無機鹽雜質氯化鈉、碳酸鈉、硫酸鈉均為分析純試劑。其中碳酸鈉和硫酸鈉的量分別以Na20C和Na2OS表示。
(二)實驗方法
將分解槽中水浴溫度升到65℃,分別向4個槽中加入1L已配置好的鋁酸鈉溶液,并根據實驗要求向各個槽中加入不同量的無機鹽,用玻璃棒攪拌使其溶解,再各加晶種500g,密封,在120r/min轉速下攪拌并開始計時,分解時間到9、21、33 h時分別降溫10、5、5℃。每隔一定時間從取樣孔取樣分析(分析苛性堿、氧化鋁含量并計算溶液的分解率)。分解溫度與時間的關系如圖1所示。
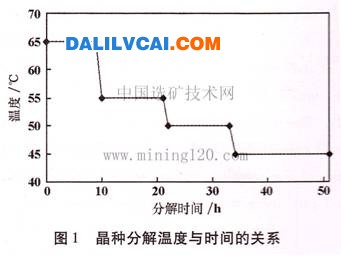
苛性堿分析采用酸堿中和滴定;氧化鋁分析采用EDTA絡合滴定法。分解率計算公式為:
![]()
式中![]() 為反應時間t小時后,鋁酸鈉溶液的分解率,%;
為反應時間t小時后,鋁酸鈉溶液的分解率,%;![]() 為反應開始時鋁酸鈉溶液的苛性分子比;
為反應開始時鋁酸鈉溶液的苛性分子比;![]() 為反應進行t小時后,鋁酸鈉溶液的苛性分子比。
為反應進行t小時后,鋁酸鈉溶液的苛性分子比。
二、結果與討論
(一)NaCl濃度對鋁酸鈉溶液晶種分解率的影響
實驗首先研究了氯化鈉濃度對鋁酸鈉溶液晶種分解率的影響,如圖2所示。
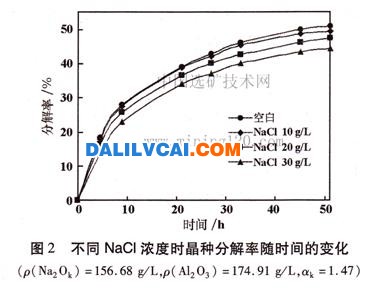
由圖2可以看出,在相同分解時間,鋁酸鈉溶液分解率隨溶液中NaCl濃度的增加而降低,NaCl濃度越高對分解率影響越大。當溶液中NaCl濃度小于10g/L時,對分解的抑制作用并不顯著;當NaCl濃度大于10g/L時,對分解有明顯的抑制作用。溶液中NaCl濃度每升高10g/L,分解率就降低約2%,當NaCl濃度為30g/L時,和空白樣品相比分解率降低了6%~7%。這是因為NaCl加入后會以簡單的鈉離子和氯離子形式存在于溶液中,晶種優先吸附簡單離子,從而降低了鋁酸根離子與晶種相互作用的能力,使晶種的活性降低。NaCl濃度較小時,氯離子在晶種表面的覆蓋度較小,不足以對鋁酸鈉溶液分解產生明顯的抑制作用,但是當NaCl濃度較大時(如濃度大于10g/L),由于氯離子在晶種表面的覆蓋度增大,鋁酸鈉溶液分解過程就會受到明顯的抑制作用。
(二)Na2S04濃度對鋁酸鈉溶液晶種分解率的影響
實驗研究了硫酸鈉(以Na2OS計)濃度對鋁酸鈉溶液晶種分解率的影響,如圖3所示。
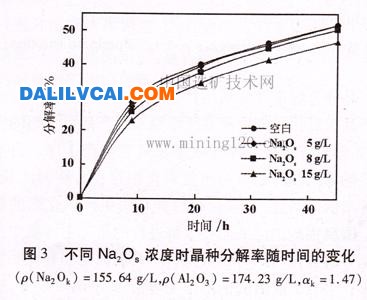
由圖3可以看出,在相同分解時間,鋁酸鈉溶液的分解率隨溶液中Na2OS濃度的增加而降低,當Na2OS濃度小于5g/L時,對分解的抑制作用不顯著;當Na2OS濃度大于5g/L時,對分解有明顯的抑制作用,且隨著Na2OS濃度的增大,對分解率的抑制作用逐漸增大。硫酸鈉抑制鋁酸鈉溶液分解的原因,可用其對溶液中A1203平衡溶解度的影響來說明。根據Misra-White平衡溶解度方程:
![]()
在溫度不變時,硫酸鈉(Na2OS)含量增大可使ρ(Na2OS)/T項增大,從而增加了氧化鋁在鋁酸鈉溶液中的平衡溶解度,導致溶液的過飽和度(C-C∞)降低,從而減小了分解過程的推動力。由圖3還可以看出,溶液中Na2OS濃度一定時,在分解前期對種分分解率的影響要大于后期,這是因為在分解前期,溶液的過飽和度大,晶種具有較好的活性和較多的高能點,分解速率快,Na2S04加入后會以簡單離子形式優先吸附在晶種表面,阻礙鋁酸根離子與晶種的相互作用,從而影響鋁酸鈉溶液的分解。在分解后期,隨著分解深度的增加,溶液過飽和度降低,分解推動力減小,分解速率下降,硫酸鈉對鋁酸鈉分解的影響程度降低。因此分解后期硫酸鈉對鋁酸鈉溶液分解率的抑制程度要小于分解前期。
(三)Na2C03濃度對鋁酸鈉溶液晶種分解率的影響
實驗研究了碳酸鈉(以Na2OC計)濃度對鋁酸鈉溶液晶種分解率的影響,如圖4所示。
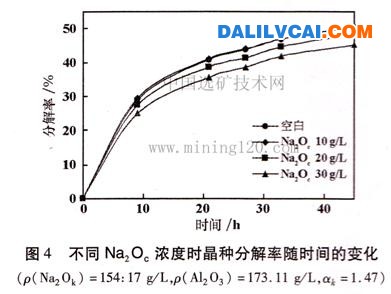
由圖4可以看出,在相同分解時間,鋁酸鈉溶液分解率隨溶液中Na20C濃度的增加而降低。在Na20C濃度為10g/L時,在21,33,45h時溶液分解率分別比空白樣高0.23%,0.21%,0.33%,可見當Na2OC濃度小于10g/L時,對晶種分解不會產生抑制作用;當Na20C濃度大于10g/L時,則會對鋁酸鈉溶液晶種分解產生明顯的抑制作用,如Na20C的濃度為30g/L時,相比空白樣而言,分解率下降了5%~6%。Na20C與Na20S的作用相類似,即當Na2S04和Na2 C03加入后會以簡單的離子形式存在于溶液中,晶種優先吸附簡單離子,使晶種的活性降低,從而影響溶液分解。當濃度較小時,離子在晶種表面的覆蓋度較小,不足以對鋁酸鈉溶液分解產生明顯的抑制作用,但當濃度較大時,離子在晶種表面的覆蓋度增大,鋁酸鈉溶液分解過程就會受到明顯的抑制作用。
綜上所述,這3種無機鹽離子對鋁酸鈉溶液晶種分解率的影響具有相同的規律,當濃度較小時,對分解的影響程度較小,隨著濃度的增加,均對分解產生明顯的抑制作用。分析其原因,一方面這3種無機鹽加入后,均以簡單的離子存在于溶液中,晶種將優先吸附簡單離子,被吸附的離子覆蓋在晶種表面上,從而阻礙了晶種與鋁酸根離子的作用,隨著無機鹽濃度增加,這種阻礙作用進一步加強;另一方面,無機鹽的存在都會增加鋁酸鈉溶液中氧化鋁的平衡溶解度,從而降低溶液的過飽和度,減少分解過程的推動力。
三、無機鹽雜質對鋁酸鈉溶液晶種分解的作用機理
(一)無機鹽對Al(OH)3表面Zeta電位的影響
將αk=3.00的鋁酸鈉溶液加去離子水稀釋到pH=12,取100mL分別加入7個燒杯中,依次編為1#~7#,1#為不加無機鹽的空白樣品,其余的6個分別加入不同量的指定無機鹽,攪拌使其溶解,再在每個燒杯中分別加入晶種A1(OH)3固體20g,攪拌2min,然后靜置15min,用JS94H微電泳儀測定Al(OH)3顆粒Zeta電位。圖5及圖6為不同NaCl、Na20C、Na2OS濃度下,鋁酸鈉溶液中Al(OH)3顆粒表面Zeta電位的變化情況。
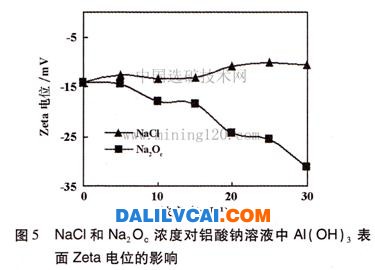
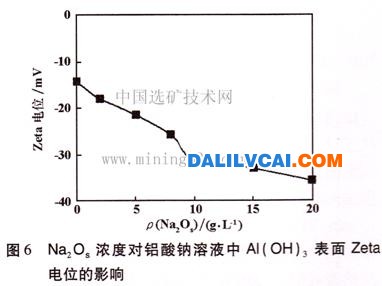
Zeta電位是描述顆粒表面電荷性質的一個物理量,它是距離顆粒表面一定距離處的電位。由圖5及圖6可以看出,NaCl的加入對鋁酸鈉溶液中氫氧化鋁顆粒的Zeta電位的影響不顯著,Zeta電位變化很小,而Na2C03和Na2S04的加入對Zeta電位的影響非常顯著,使Zeta電位變得更負。溶液中加入無機鹽后,其陰離子會和氫氧化鋁晶體顆粒表面的A1(OH)4-發生離子交換,由于碳酸根離子和硫酸根離子所帶電荷均為2價,隨著濃度的增大,離子交換量也增大,晶種表面的電位將發生顯著改變,使Zeta電位變得更負;而氯離子所帶電荷為一價,由于離子交換而導致Zeta電位隨NaCl濃度的變化并不顯著。由圖5及圖6還可以看出,硫酸鈉對溶液中氫氧化鋁顆粒Zeta電位值的變化要比碳酸鈉對氫氧化鋁顆粒Zeta電位值的變化更加明顯,如Na2OS濃度為20g/L時,Zeta電位值為-35.6324mV,而Na2OC濃度為20g/L時,Zeta電位值為-24.4273mV。這可能是因為硫酸根和碳酸根這2種離子的結構不同而導致的,硫酸根離子為正四面體結構,碳酸根為正三角形結構,在鋁酸鈉溶液中鋁酸根主要以四面體Al(OH)4-形態存在,由相似原理可知,硫酸根離子更容易與鋁酸根離子發生離子交換,因此,Zeta電位值隨硫酸鈉的變化更顯著。Zeta電位是一個影響固一液界面性質的重要參數,而鋁酸鈉溶液晶種分解又是在固一液界面進行的,因此,Zeta電位將直接影響鋁酸鈉溶液晶種分解。無機鹽的存在使Zeta電位變得更負,不利于氫氧化鋁晶體顆粒對鋁酸根離子的吸附,從而對鋁酸鈉溶液晶種分解產生的抑制作用。
(二)無機鹽對鋁酸鈉溶液表面張力的影響
取100mL配制好的鋁酸鈉溶液(ρ(Na2O)=153.48g/L;ρ(A1203)=170.63g/L;αk=1.47)分別加入7個燒杯中,依次編為1#~7#,1#為不加無機鹽的空白樣品,其余的6個分別加入不同量的指定無機鹽,攪拌使其溶解,用DT-102型全自動界面張力儀測試溶液表面張力,圖7及圖8為NaCl、Na20C、Na20S不同濃度時,鋁酸鈉溶液的表面張力變化情況。
由圖7及圖8可以看出,無機鹽對鋁酸鈉溶液表面張力有一定的影響,隨著無機鹽濃度的增加,溶液表面張力增大。從分子觀點來看,表面張力是一個與表面平行并力圖使表面收縮的力。表面張力的降低會使溶液在晶體表面的潤濕性變好,更有利于離子在固體表面的鋪展,同時也會使臨界成核半徑減少,二次成核加快,反之則會對分解產生不利影響。
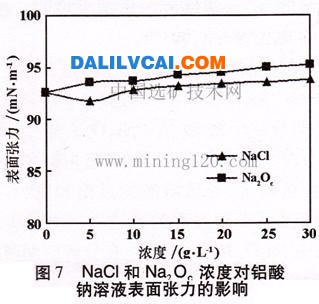
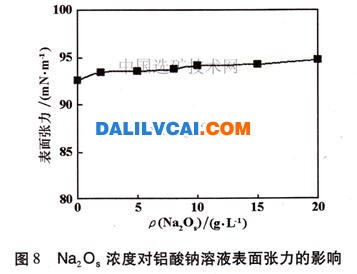
晶種分解時,鋁酸鈉溶液中的鋁酸根離子是在晶種氫氧化鋁表面以氫氧化鋁顆粒為成核中心成核,這個過程包括:①鋁酸根離子向氫氧化鋁顆粒表面擴散;②在顆粒表面吸附;③核的長大與脫離。因此,吸附是成核的必要條件。而電解質溶液中的吸附具有以下規則:①選擇與吸附體類似的溶質;②選擇與吸附體晶格大小類似的離子;③選擇在吸附體表面上生成難溶或不溶的離子。在鋁酸鈉溶液中,鋁酸根離子存在形態復雜,離子團較大。因此,氫氧化鋁晶體顆粒會優先吸附簡單的無機鹽離子。同時無機鹽的存在使鋁酸鈉溶液表面張力增大,使溶液在晶體表面的潤濕性變差,阻礙鋁酸根離子的吸附,從而對晶種分解產生抑制作用。
四、結論
(一)鋁酸鈉溶液中氯化鈉、碳酸鈉、硫酸鈉等雜質的存在對晶種分解會產生不利影響。當NaCl濃度大于10g/L,Na20S濃度大于5g/L,Na20C濃度大于10g/L時,均將對鋁酸鈉溶液晶種分解產生明顯的抑制作用。
(二)Zeta電位直接影響鋁酸鈉溶液晶種分解。無機鹽雜質的存在會影響鋁酸鈉溶液中氫氧化鋁顆粒表面的Zeta電位值,使Zeta電位變得更負,不利于氫氧化鋁晶體顆粒對鋁酸根離子的吸附,從而對鋁酸鈉溶液晶種分解產生抑制作用。
(三)無機鹽雜質使鋁酸鈉溶液表面張力增大,也阻礙鋁酸根離子在晶體表面的吸附,對晶種分解產生不利影響。





